Ramon Devesa Such retweetledi

Nefrotoxicidad por contraste en 2026 — ¿realmente este debate ya terminó?
Florens y Demiselle publicaron una revisión convincente en Kidney360 (7:445–449, 2026) en la que argumentan que el riesgo de lesión renal aguda inducida por contraste (CI-AKI) ha sido sobreestimado durante décadas y que el “renalismo” —evitar estudios de imagen indicados por miedo— causa más daño que el propio contraste.
Tienen razón en parte. Pero la historia es más matizada de lo que sugiere el título, y los cardiólogos intervencionistas deberían leerlo con atención, aunque no de forma acrítica.
La evidencia sobre la seguridad del contraste intravenoso es ahora robusta. McDonald et al. (Radiology 2013) estudiaron 53,439 pacientes con ajuste por propensión Y un análisis contrafactual. El OR de LRA tras TAC con contraste vs. sin contraste fue de 0.92 (IC 95% 0.75–1.13). Ehmann et al. (Intensive Care Medicine 2023) fueron más allá: 14,449 pacientes con LRA preexistente al ingreso en urgencias. OR ponderado por propensión para LRA persistente con contraste: 0.93 (IC 95% 0.83–1.05). Sin aumento de diálisis a 180 días. Incluso en pacientes que ya tenían LRA, el contraste IV no empeoró los desenlaces.
En cuanto a prevención, PRESERVE (NEJM 2018) enterró definitivamente el bicarbonato y la N-acetilcisteína —GRACIAS A DIOS—: ninguno funcionó en 5,177 pacientes de alto riesgo. AMACING (Lancet 2017) mostró que no hidratar fue no inferior a hidratar en pacientes con TFGe 30–59, y que la hidratación misma causó insuficiencia cardiaca en el 4% de los pacientes. Estábamos tratando un problema que casi no existe con intervenciones que no funcionan y que a veces causan daño.
Hasta aquí, la tesis se sostiene. Para el contraste IV y la tomografía, el miedo a la CI-AKI es en gran medida infundado con los agentes modernos.
Pero aquí está lo que me incomoda (y donde creo que la revisión exagera): extrapola datos de TAC/contraste IV al contexto de cateterismo sin reconocer adecuadamente que son escenarios clínicos fundamentalmente distintos.
En la tomografía, se administra contraste IV de 80–120 mL, con hemodinamia estable, sin manipulación arterial ni ateroémbolos. Tasa basal de LRA: 2–4%. En el laboratorio de hemodinamia, hay exposición intraarterial de primer paso renal, frecuentemente 150–300+ mL de contraste, manipulación arterial que puede embolizar colesterol hacia las arterias renales, inestabilidad hemodinámica, sangrado y, en ocasiones, soporte circulatorio mecánico. Tasas de LRA: 7–57% según el perfil de riesgo de Mehran.
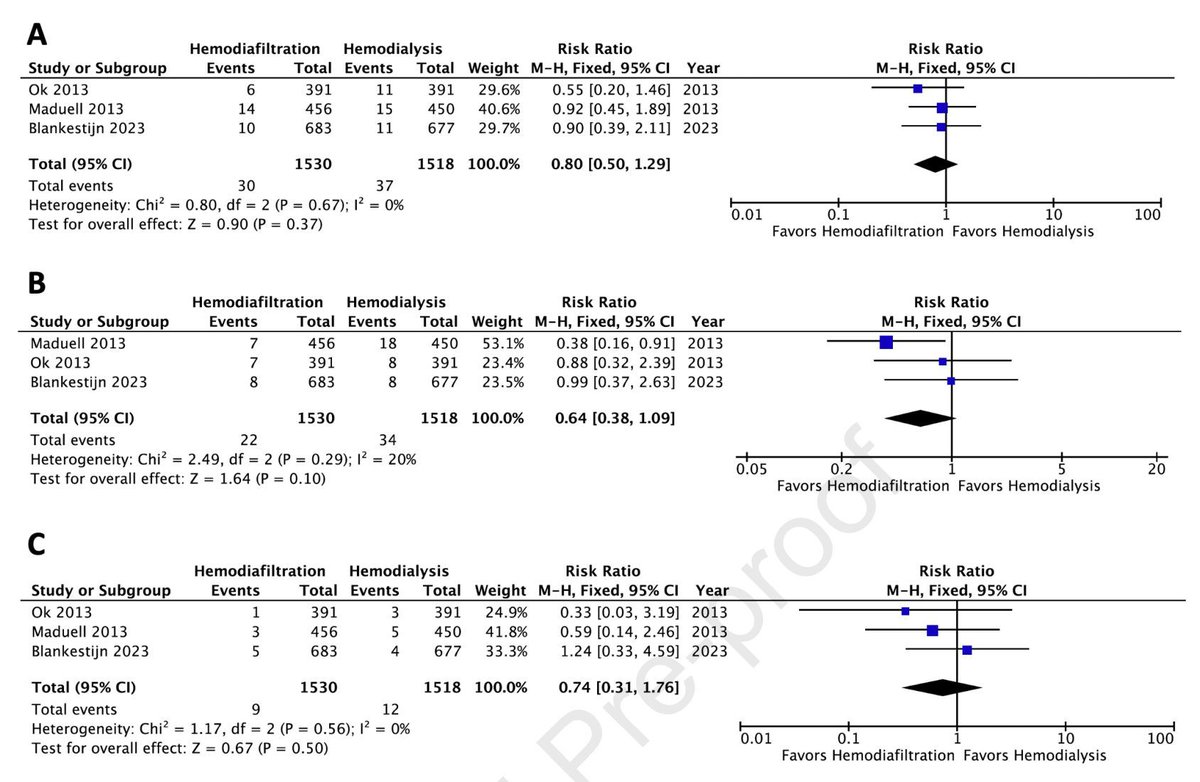
POSEIDON (Lancet 2014) nos dio una pista de que algo sí ocurre. La hidratación guiada por la presión telediastólica del VI redujo la CI-AKI de 16.3% a 6.7% en el contexto de cateterismo cardiaco —una reducción relativa del 59% (RR 0.41, IC 95% 0.22–0.79). Si el contraste fuera irrelevante en este entorno, ¿por qué la expansión de volumen —que diluye el contraste, aumenta el flujo urinario y reduce el tiempo de exposición tubular— disminuiría la LRA? Algo SÍ está pasando en el contexto del cateterismo.
El score de riesgo de Mehran (JACC 2004) cuenta la misma historia desde otro ángulo. Hipotensión: 5 puntos, uso de balón intraaórtico: 5, insuficiencia cardiaca: 5, edad >75: 4 — el volumen de contraste aporta solo 1 punto por cada 100 mL. El score no identifica al contraste como LA causa de LRA post-ICP; lo integra dentro de una constelación de riesgo junto con compromiso hemodinámico, complejidad del procedimiento y vulnerabilidad basal. La LRA tras cateterismo es un síndrome multifactorial, no un evento puro de toxicidad por contraste.
En realidad, todos los estudios con emparejamiento por propensión que muestran “ausencia de daño” comparten la misma limitación: confusión por indicación. Los clínicos evitan sistemáticamente el contraste en pacientes más graves. La cohorte de UCI de Berglund (European Radiology 2024) lo demuestra claramente: el grupo sin contraste tenía creatinina basal de 100 vs. 77 µmol/L, cuatro veces más
Español