Sabitlenmiş Tweet

OpenAI의 생명과학 보고서: AI는 어떻게 신약 개발을 가속시키는가
-
신약 개발의 생산성 저하와 이룸의 법칙(Eroom's Law)
지난 100년 동안 의학은 큰 발전을 이루었지만 신약을 하나 개발하는 데 드는 비용은 9년마다 두 배씩 늘어나고 있습니다. 이를 반도체 성능이 비약적으로 발전한다는 무어의 법칙을 뒤집은 이룸의 법칙(Eroom's Law)이라고 부릅니다.
실제로 1950년대와 비교하면 신약 생산성은 약 80배나 줄어들었으며, 현재 신약 하나를 만드는 데는 약 26억 달러의 막대한 비용과 12년에서 15년이라는 긴 시간이 소요됩니다. 임상 1상에 진입한 후보 물질이 최종 승인을 받을 확률도 7.9%에 불과할 정도로 성공 문턱이 매우 높습니다.
-
지식의 파편화와 지식의 암흑기(The Great Endarkenment)
신약 개발이 어려워진 근본 원인은 기술 부족이 아니라 지식이 너무 세분화되어 서로 연결되지 않기 때문입니다. 생물학은 유전학, 단백질 생화학, 면역학 등 20개 이상의 분야로 나뉘어 있고 각자 사용하는 용어가 달라 소통이 어렵습니다.
OpenAI는 이를 지식의 과도한 분화로 인한 이해 단절, 즉 지식의 암흑기(The Great Endarkenment)라고 정의했습니다. 하지만 최근에는 인간의 몸을 구성하는 DNA를 4개의 문자로 된 디지털 코드로 읽을 수 있게 되었고, 유전자 편집 기술인 크리스퍼(CRISPR)를 통해 이를 직접 수정하는 단계까지 발전했습니다.
-
단백질 구조 예측과 분자 설계의 혁신
단백질의 입체 구조를 알아내는 것은 신약 개발의 핵심이지만 과거에는 실험을 통해 하나를 밝히는 데만 수개월에서 수년이 걸렸습니다. 하지만 구글의 알파폴드(AlphaFold) 같은 인공지능 모델은 50년 동안 풀리지 않았던 이 난제를 해결하며 2억 개 이상의 단백질 구조를 한 번에 예측해냈습니다. 이는 기존 방식으로는 수억 년이 걸렸을 작업을 단 몇 년 만에 끝낸 것과 같은 효과를 주며, 약물 분자가 질병 유발 인자에 얼마나 잘 결합할지를 사전에 계산할 수 있게 만들어 연구 속도를 획기적으로 높였습니다.
$ABSI $GENB $프로티나(Proteina)
-
유전자 편집 기술의 진화
인공지능은 단순히 기존의 유전자 편집 도구를 사용하는 것을 넘어 자연계에 존재하지 않는 새로운 유전자 편집 효소 자체를 설계하기도 합니다. 크리스퍼(CRISPR-Cas9) 기술이 특정 DNA를 잘라내는 수준이었다면, 이제는 단일 염기만 바꾸거나 더 긴 서열을 수정하는 정교한 단계로 발전했습니다. 특히 2025년 연구에 따르면 대규모 언어 모델(LLM)이 설계한 유전자 편집 도구가 자연 상태의 효소보다 더 뛰어난 성능을 보이기도 하며 생명체의 설계도를 더 정확하게 수정할 수 있게 되었습니다.
$TXG $CRSP $BEAM $프로플루언트(Profluent)
-
자동화 연구실의 등장 (Self-driving lab)
기존에는 사람이 직접 가설을 세우고 실험과 분석을 반복해야 했기에 한 번의 사이클에 수개월이 걸렸습니다. 하지만 인공지능과 로봇이 결합한 자동화 연구실은 설계부터 실험, 분석에 이르는 전 과정을 스스로 수행합니다. 이를 통해 연구 사이클이 수일 수준으로 단축되었으며, 실제 일부 기업은 신약 타겟을 찾고 임상 1상에 진입하기까지의 기간을 30개월 이하로 대폭 줄이는 성과를 보여주고 있습니다.
$DNA $RXRX
-
임상 시험 최적화 및 효율성 개선
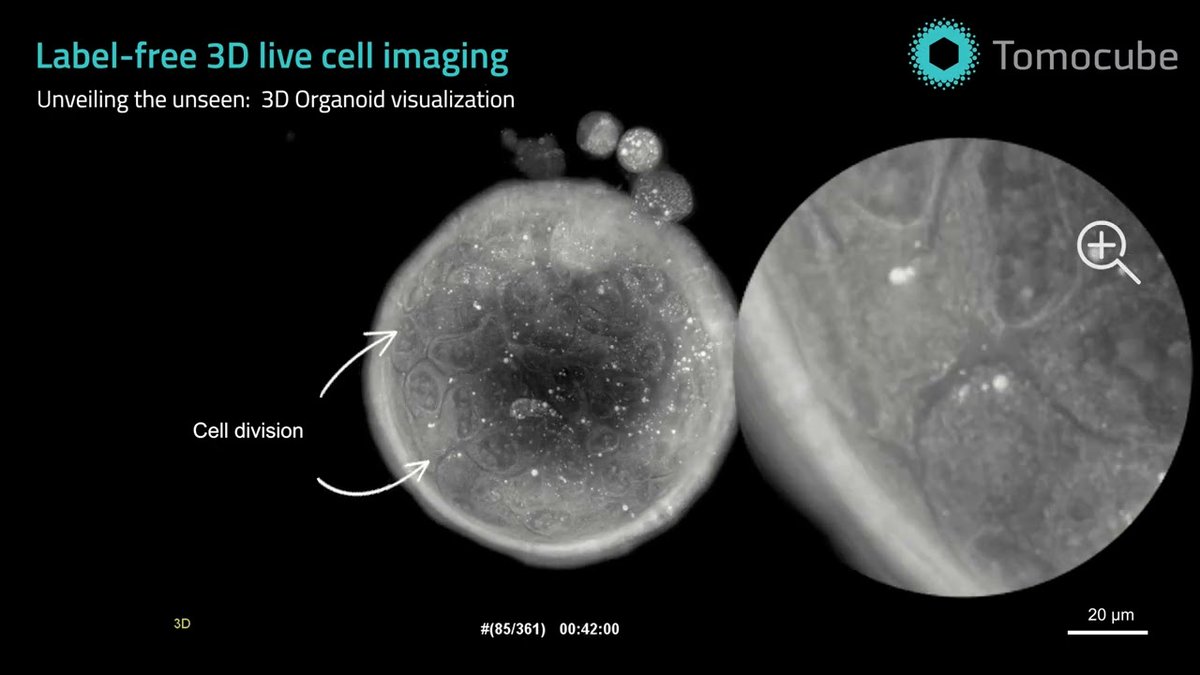
임상 시험은 신약 개발에서 가장 오래 걸리고 실패율이 높은 구간이지만, 인공지능은 환자 모집부터 안전성 모니터링까지 전 단계를 최적화합니다. 방대한 데이터를 분석해 약이 잘 들을 것 같은 환자 그룹을 미리 분류하고 실패 가능성이 높은 시험을 조기에 걸러냄으로써 병목 현상을 해결합니다. 일부 분석에 따르면 이러한 기술 적용을 통해 임상 단계에 소요되는 기간을 20% 이상 단축할 수 있는 것으로 나타났습니다.
$TEM $토모큐브(Tomocube)
-
인공지능의 역할: 지식의 번역기와 폴리매스(Polymath)
결국 인공지능은 생명과학의 특정 단계만 돕는 도구가 아니라 서로 다른 분야의 지식을 연결해주는 번역기 역할을 합니다. 과거에는 여러 분야에 능통한 소수의 천재인 폴리매스(Polymath)가 했던 역할을 인공지능이 대신하면서, 연구자가 자기 분야가 아닌 지식도 쉽게 이해하고 활용할 수 있게 되었습니다.
OpenAI는 인공지능이 데이터를 읽고 분석하며 실험하고 다시 학습하는 전체 연구 순환 과정을 하나로 묶는 거대한 인프라로 자리 잡으며 생물학 연구의 판도를 바꾸고 있다고 강조합니다.

한국어